Látky se skládají z částic, které vykonávají neustálý, neuspořádaný pohyb, tzv. tepelný pohyb. Mění svoji polohu, ale také kmitají okolo svých rovnovážných poloh. Zajímá nás proto jejich potenciální a kinetická energie.
Těleso, které je v klidu se navenek jeví, že nemá žádnou energii. Jeho částice se ale v tělese stále pohybují, mají proto energii, kterou nazýváme vnitřní energie tělesa. Označujeme ji U, její jednotkou je joule.
Vnitřní energie tělesa je součet celkové polohové a pohybové energie částic, ze kterých je těleso složeno.
Protože u pevných látek převažují hlavně přitažlivé síly nad pohybem částic, tvoří jejich vnitřní energii hlavně polohová energie atomů a molekul. U plynů se ale částice pohybují velkými rychlostmi, proto vnitřní energii tvoří hlavně kinetická energie částic.
Vnitřní energie tělesa není veličina stálá, můžeme ji měnit konáním práce na tělese (působením vnější silou) nebo tepelnou výměnou (zahříváním nebo ochlazováním).
Jestliže těleso budeme stlačovat nebo roztahovat, ohýbat, třít po podložce nebo zatloukat, tak se konala práce, o kterou se zvýšila vnitřní energie tělesa. Budeme-li těleso ohřívat nebo ochlazovat, bude se vnitřní energie tělesa měnit tepelnou výměnou. Změnu vnitřní energie označujeme ΔU.
`∆U = U_2 - U_1`
`i`
U1… počáteční energie, před konáním práce nebo tepelnou výměnou
U2 …energie na konci děje, po konání práce nebo tepelné výměně
Změna vnitřní energie konáním práce
Když vnější silou působíme na píst a budeme tak stlačovat plyn uzavřený ve válci, zmenší se vzdálenosti mezi částicemi plynu a tím jeho objem (nastala změna polohové energie částic). Částice začnou na píst a na stěny válce dopadat rychleji (změnila se pohybová energie částic) a častěji, vzroste tlak plynu. Nastala změna vnitřní energie plynu vyvolaná vnější silou F, která posunutím pístu o vzdálenost s, vykonala mechanickou práci W. Vykonaná práce se projevila zvýšením vnitřní energie plynu a materiálu ze kterého je válec vyrobený. Vzrostla teplota soustavy válec - plyn.
Změna vnitřní energie způsobená konáním práce se projeví zvýšením teploty nádoby a stlačovaného plynu.

Obr. 26: Částice v plynu před stlačením
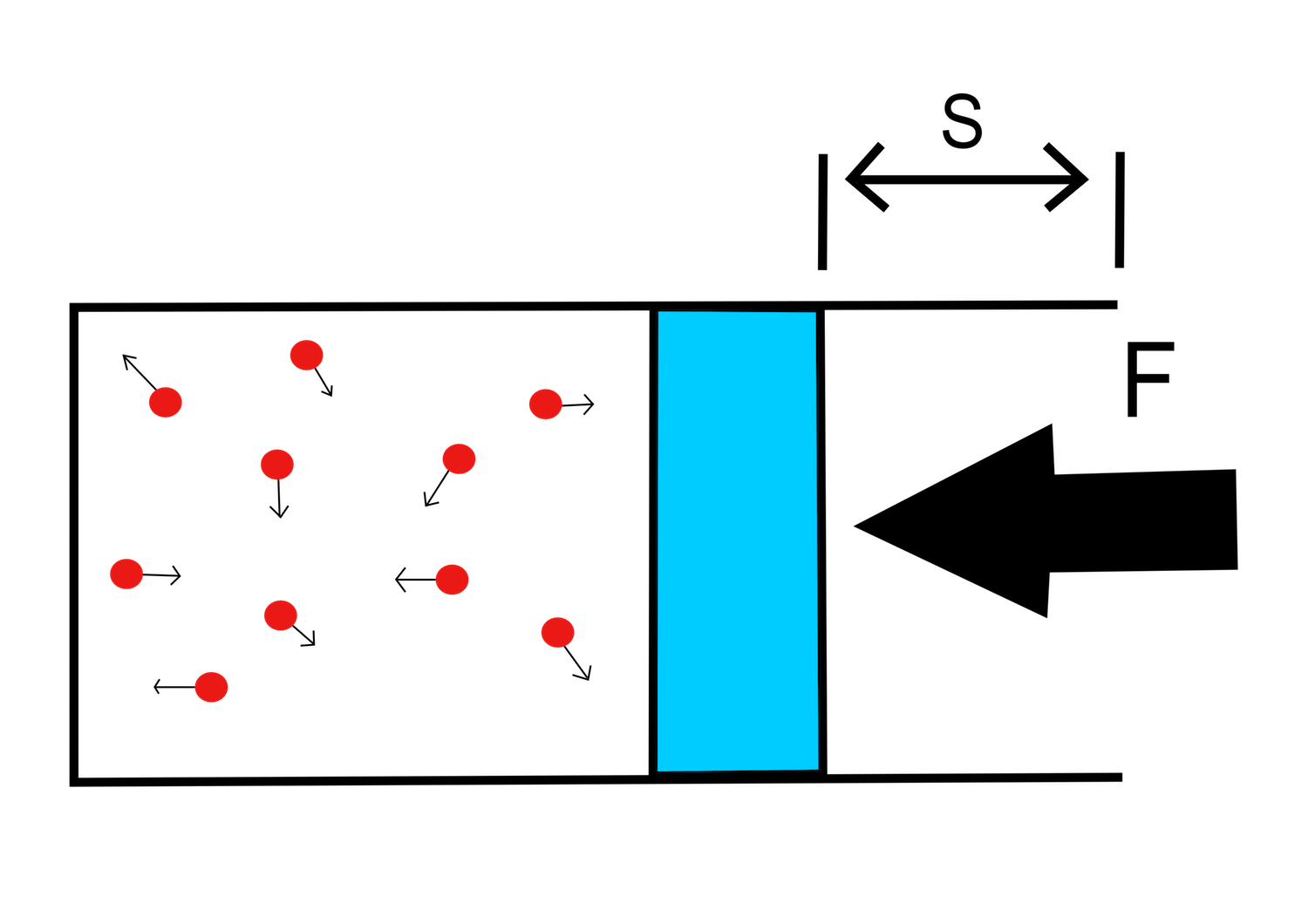
Obr. 27: Částice v plynu po stlačení
Když budeme plnit hustilkou prázdnou PET láhev, vzroste počet molekul vzduchu uvnitř objemu láhve, částice budou blízko sebe a budou se vzájemně častěji srážet, vzroste jejich rychlost a tlak na stěny láhve. Nastala změna vnitřní energie soustavy PET láhev – vzduch, kterou poznáme ze zvýšené teploty vzduchu uvnitř láhve.
Další příklady změny vnitřní energie těles konáním mechanické práce:
- Při obrábění kovů se zvětšuje vnitřní energie kovu a nože.
- Povrch letadel se za letu ohřívá třením o vzduch.
- Meteoroid letící atmosférou Země se za letu ohřívá, někdy v atmosféře shoří.
Změna vnitřní energie tepelnou výměnou
Dotýkají-li se dvě tělesa o různých teplotách, dochází k vzájemným srážkám částic z obou těles. Částice teplejšího tělesa, s větší kinetickou energií, předají část své vnitřní energie částicím z tělesa chladnějšího.
Jestliže se vnitřní energie jednoho tělesa zvýší na úkor vnitřní energie druhého tělesa, říkáme, že mezi tělesy nastala tepelná výměna.
Tepelná výměna bude probíhat tak dlouho, dokud se teploty obou těles nevyrovnají.
Vnitřní energie se může tepelnou výměnou změnit i mezi tělesy, která se vzájemně nedotýkají. Zvýšení teploty tělesa umožňuje tepelné záření.
Když teplejší těleso odevzdá tepelnou výměnou studenějšímu tělesu energii, říkáme, že teplejší těleso odevzdalo studenějšímu tělesu teplo. Teplo, ale není vnitřní energie tělesa. Vnitřní energie, totiž charakterizuje stav tělesa, zatímco teplo děj, který probíhá mezi tělesy. Nemůžeme tedy říkat, že tělesa v sobě obsahují teplo.
První termodynamický zákon
V životě se velmi málo setkáváme s ději, při kterých se vnitřní energie těles mění jen jedním způsobem- tepelnou výměnou nebo konáním práce. Většinou je možné jejich vnitřní energii změnit oběma možnostmi. Plyn uzavřený ve válci můžeme stlačovat pístem a současně zahřívat, při jízdě autem se pneumatika zahřeje třením o silnici a současně tepelným zářením ze Slunce. Na základě těchto zkušeností můžeme formulovat první termodynamický zákon, který hovoří o změně vnitřní energie tělesa.
Změna vnitřní energie je rovna součtu práce vykonané okolními tělesy, které působily na soustavu a tepla odevzdaného okolními tělesy soustavě.
ΔU = W + Q
ΔU… změna vnitřní energie
W… práce vnějších sil
Q … teplo dodané do soustavy
Soustava může:
-
přijmout energii od okolních těles
ΔU = W + Q
nebo
-
může energii okolním tělesům odevzdávat.
Q = ΔU + W
ΔU… změna vnitřní energie soustavy
W… práce, kterou soustava vykoná
V prvním případě jsou práce a teplo dodané do soustavy veličiny kladné, ve druhém případě jsou záporné.
- W > 0….. vnější síly konají práci Q > 0 ….. soustava přijala teplo od jiného tělesa
- W < 0….. soustava koná práci Q < 0 ….. soustava odevzdala teplo jinému tělesu
Můžeme se ale setkat se dvěma zvláštními případy, které vyplynou z 1. termodynamického zákona.
1) Q = 0
Vnitřní energie soustavy se změní jen konáním práce, kterou na ní vykonaly vnější síly.
ΔU = W
2) W=0
Vnitřní energie soustavy se změní jen dodaným teplem, které ji dodají okolní tělesa.
ΔU = Q
Teplo Q dodané soustavě se spotřebuje na změnu vnitřní energie ΔU soustavy a práci W, kterou soustava vykoná. Když se soustava vrátí do původního stavu (proběhne tzv. kruhový děj), je změna vnitřní energie soustavy ΔU = 0. Potom z prvního termodynamického zákona vyplývá
`Q=W`
Teplo dodané soustavě se spotřebuje jen na vykonání práce. Tato práce nemůže být větší než teplo, které bylo dodané soustavě. Proto žádný stroj nemůže vykonat víc práce, než byla velikost energie, kterou jsme do stroje vložili.
Nelze sestrojit perpetuum mobile prvního druhu.
Perpetuum mobile je zařízení, které by mělo trvale konat práci, aniž by z okolí čerpalo energii. Takové zařízení dosud nebylo vynalezeno a podle stanoviska současné vědy, ani vynalezeno být nemůže. Odporuje první větě termodynamické a tím zákonu zachování energie. Z prvního termodynamického zákona to můžeme snadno dokázat.
1. termodynamický zákon ......................... Δ U = W + Q
Obr. 28: Představa perpetua mobile
Obr. 29: Představa perpetua mobile
Perpetuum mobile by mělo trvale pracovat, stroj se musí vždy znovu vrátit do svého původního stavu. Změna vnitřní energie v takovém stroji je nulová ΔU = 0. Perpetuum mobile musí mít stejnou hodnotu vnitřní energie na začátku a na konci. Protože nepřijímá žádnou energii z okolí, nemůže přijmout ani teplo Q. V rovnici 1. termodynamického zákona je proto teplo Q = 0.
Celý 1. termodynamický zákon se tím upraví do tvaru 0 = W + 0. Z rovnice je vidět, že práce, kterou stroj vykoná, bude rovna nule. Nelze sestrojit perpetuum mobile.
Skutečnost, že konáním mechanické práce je možné získat velké množství tepla, poprvé ověřil Benjamin Thompson, hrabě Rumford (1753 – 1814), který vložil bronzový válec, ve kterém se měl vyvrtat otvor pro dělovou hlaveň, do nádoby se 13 litry ledové vody. Při vrtání ocelovým vrtákem vzniklo tolik tepla, že se voda za 2,5 hodiny uvedla do varu. Souvislost práce a tepla poprvé správně vystihl J. R. Mayer, který dospěl k zákonu zachování energie. Tento zákon přesně a jasně formuloval H. Helmholtz.
ŘEŠENÉ ÚLOHY
Úloha č. 1 
Úloha č. 2 
Úloha č. 3 - Řekni, s použitím správných fyzikálních pojmů, celé znění prvního termodynamického zákona.
Úloha č. 4 - Jakými způsoby můžeme zvýšit vnitřní energii plynu ve válci, který je uzavřený pohyblivým pístem?
Úloha č. 5 - Uveď alespoň tři příklady, ve kterých dojde ke změně vnitřní energie plynu konáním mechanické práce.
